- 收藏
- 加入书签
石蜡油分解实验的新设计
【摘要】 催化剂改进方面用二氧化锰代替碎瓷片,从安全性的角度采用安全瓶改进课本实验装置,从反应药品常见性角度用固体石蜡代替课本上沾有石蜡油的矿渣棉。将课本难以成功的科学探究演示实验改进为学生分组实验,现象明显,操作简单,安全性和成功率高。
【关键词】 石蜡油 实验改进 措施
【中图分类号】 G633.8 【文献标识码】 A 【文章编号】 1992-7711(2020)03-171-020
1.课本实验难成功原因
人教版必修2课本(第67页)第三章第二节引入了石蜡油分解实验,其实验装置图如下图1。其原理是利用石蜡油蒸汽遇到灼热的碎瓷片,分解产生乙烯等气体,可分别使溴水和酸性高锰酸钾等溶液褪色。目的是让学生通过该实验了解到乙烯来自于石油,并通过实验调动起学生学习的兴趣,让学生主动探究乙烯的性质。培养学生科学探究和创新意识,符合化学学科核心素养的要求。但该实验成功率很低,即使成功,所需时间也太长,耗时约7~10分钟。绝大多数老师采取看视频的方式代替该演示实验。这在一定程度上影响了演示实验的开展,影响了学生对知识的可信度和学生科学探究的积极性。
笔者在实验中将浸透石蜡油的矿渣棉放在试管最里端,碎瓷片放在试管中部,在碎瓷片下方用酒精灯加热,预计石蜡油气化,产生的石蜡油蒸气外逸,遇到高温碎瓷片发生分解,产生不饱和烃使溴水或酸性高锰酸钾溶液褪色。该实验的目的,主要是说明产物中含有与烷烃性质不同的烃——烯烃。此实验存在如下的问题:
1.1药品不常见石蜡油和矿渣棉在普通中学实验室不常见,学生感到很陌生,无法提起学生的兴趣。
1.2成功率低一方面,由于酒精灯在碎瓷片下方加热,石棉能吸附的石蜡油量较小,石蜡油汽化的温度(390~405℃)较石蜡油分解温度(约为450~560℃)低,结果石蜡油多数都已经变为蒸气逸出,碎瓷片温度还尚未能升至石蜡分解所需温度,而当碎瓷片温度升至足够石蜡分解温度时,石蜡已大部分气化并逸出装置,由于剩余的石蜡量少,气化后遇碎瓷片分解产生烯烃的速率慢,产生烯烃的总量小。另一方面,在原装置中,由于液体石蜡油并非主动受热,更导致由此产生的蒸汽量很少,所以当极少量的石蜡油蒸汽再通过灼热的碎瓷片时,分解产生的乙烯等气体将更少,上述二方面的原因都导致溴水或酸性高锰酸钾溶液褪色所需时间较长或不能完全褪色,无法达到实验目的,因此存在实验成功率低。
1.3催化剂催化效率低笔者查阅资料得知,催化剂的活性取决于其组成和结构,碎瓷片由于含有氧化铝,所以能起催化作用,但因为碎瓷片结构致密,气孔率低,故其催化效果不理想,而教材采用碎瓷片做为本实验的催化剂可能是因为其常见而已。故笔者在本文中要寻找理想的催化剂代替碎瓷片。
1.4装置安全性不够本实验产生的裂化气很少,右边试管内的溶液容易倒吸进入硬质试管中。教材中要求将“浸透了石蜡油的石棉放置在硬质试管的底部,以保证实验的原料的量足够多,保证生成的烯烃能使小试管两种溶液分别褪色,最后剩余气体能燃烧。但教材的装置图的试管是平放的,这就造成一个缺点,若石蜡油过多,则易流动到催化剂碎瓷片上,但若把试管中略向上倾斜,则催化剂碎瓷片易在重力的作用下滑落到试管底部。所以如何解决石蜡油的用量与装置操作上的矛盾呢?
2.实验改进
2.1操作
连接好实验装置图,检查装置的气密性,装好二氧化锰和石蜡油的糊状物,用两个试管分别准备好酸性高锰酸钾溶液和溴水,先预热后对准药品加热,将导管依次通入装好酸性高锰酸钾和溴水的试管。观察现象。
2.2实验改进的关键
2.2.1药品将石蜡油和矿渣棉改为石蜡
石蜡油,生活中不常见,学生感到陌生。关于石蜡油的研究并不多,刘炳义主编的《中国石油化工商品手册》中没有记载,只能在马世昌主编的《化工产品辞典》中第88页中查到有关石蜡油的记载。石蜡油分为重质液体石蜡油和液体石蜡油两种,其主要成分是含C18~C30的正构烷烃。而石蜡可用学生所熟悉的蜡烛切取2厘米而来,其主要成分是正构和异构烷烃以及带长链基侧链的环烷烃、芳香烃等组成的混合物,分子中的碳原子数为C20~C35.烷烃在无氧条件下,在高温条件下,分子中的碳碳键和碳氢键均可断裂,由分子量大的变成分子量小的化合物,这种反应叫裂解。由于石蜡含碳原子数比石蜡油多,分子量比较大,故更易发生裂解反应,生成小分子的烷烃和烯烃。由于石蜡的熔点是57~63℃,易产生蒸气,裂解要求的温度比较低,反应速率较快,所以无需要矿渣棉。
2.2.2催化剂的改变将碎瓷片改为二氧化锰
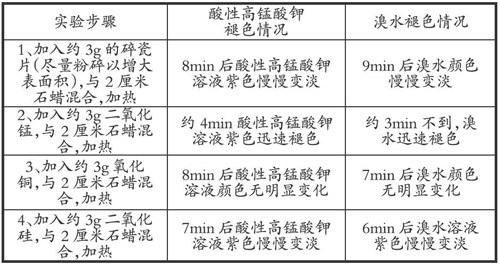
课本的实验方案中利用碎瓷片作为催化剂,但实践证明效果不佳,碎瓷片具有很高的稳定性和热容量,主要起到了蓄热升温的作用。起不到催化剂的作用。笔者尝试着换用其它催化剂,先后用了碎瓷片、二氧化锰、氧化铜、二氧化硅等。按上述图2安装好实验装置后,进行对比实验。
不同的催化剂对实验的影响
对比实验证明,二氧化锰作为本实验的催化剂催化效果最佳。只要稍稍加热一下二氧化锰和石蜡油的糊状物,马上产生大量的蒸气,使酸性高锰酸钾和溴水在不到1分钟的时间即可完全褪色。
2.2.3安全性的改进由于课本教材实验产生的蒸气不稳定,试管中的高锰酸钾溶液和溴水容易发生倒吸,进入硬质试管中,而本实验加了安全瓶,解决了倒吸的危险。同时笔者还把反应本来水平放置的试管改进垂直,优点在于解决了上述提到的石蜡油的用量与装置操作上的矛盾。
3.实验改进后的优点
改进后的实验采用了学生熟悉的蜡烛,让学生感到化学就在身边,研究化学并不神秘,这样才能引起学生对学习化学的兴趣。装置和操作都很简单并安全,所以可设计成学生分组实验,现象明显,成功率很高。课堂上可大胆地引导学生通过实验现象分析推理,让学生体验科学探究的学习过程。最后笔者要提一下本实验要成功的细节,为了更快地看到溶液褪色的现象,所采用的高锰酸钾溶液和溴水的浓度要小,为增强其氧化性,最好在配好的稀溶液中滴加2或3滴稀硫酸。同时本实验中所用到的仪器必须要先干燥,因为水能使催化剂中毒。
4.实验注意事项
1.高锰酸钾宜用稀溶液,3mL该溶液中一般加入2~3滴稀硫酸,增加溶液的氧化性;
2.溴水宜用稀溶液,也可用溴的四氯化碳溶液替代,配制溴的四氯化碳溶液时,20mL四氯化碳加1~2滴液溴即可。
[ 参 考 文 献 ]
[1]宋心琦主编.普通高中课程标准实验教科书[J].化学2(必修)[M].北京:人民教育出版社,2004:67.
[2]雷远春.2002硅酸盐材料理化性能检测.湖北:武汉理工大学出版社:7-9.
[3]邢其毅等.基础有机化学(第二版)[M].北京:高等教育出版社,2003:62.








 京公网安备 11011302003690号
京公网安备 11011302003690号


